Metode de preparare polimeri
Metode de preparare polimeri
Polimerii au fost preparate prin metode de polimerizare sau policondensare.
Polimerizare (poliadiție). Această reacție formarea polimerului prin adiția secvențială a moleculelor de substanță moleculară mică (monomer). O contribuție mare la studiul realizat de procesele de polimerizare ale oamenilor de știință noastre SVLebedev, S.S.Medvedev et al. Și cercetătorii străini G.Shtaudinger, G. Markov, K.Tsigler și colab., În polimerizarea prin produse care nu sunt formate și, prin urmare, compoziția elementară macromoleculelor diferită de compoziția moleculelor de monomer. Ca monomeri utilizați compuși cu legături multiple C = C, C = N, C = C, C = O, C = C = O, C = C = C, C = N, sau compuși cu grupări ciclice capabile dezvăluite, de exemplu:
În timpul polimerizării există o ruptură sau mai multe legături în inelul de deschidere monomeri și apariția legăturilor chimice între grupurile pentru a forma o macromoleculă, de exemplu:
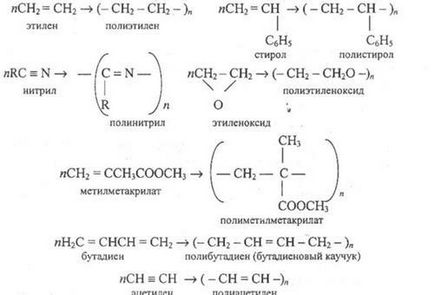
Numărul de specii monomeri care participă distinge gomopolime-polarizare (un tip de monomer) și copolimerizare (cele două sau mai multe tipuri de monomeri).
Polimerizarea - proces exoterm spontană (DG<0, DH<0 ), так как разрыв двойных связей ведет к уменьшению энергии системы. Однако без внешних воздействий (инициаторов, катализаторов и т.д.) полимеризация протекает обычно медленно. Полимеризация является цепной реакцией. В зависимости от характера активных частиц различают радикальную и ионную полимеризации.
proces este inițiat de către radicalii liberi în polimerizarea radicalică. Reacția se desfășoară prin mai multe etape: a) inițierea; b) o creștere a lanțului; c) transferul sau lanțul de terminare:
a) inițierea - formarea centrilor activi - radicali și macroradicals - are loc prin termică, fotochimică Skog, chimice, radiații sau alte influențe. In majoritatea cazurilor, inițiatorii de polimerizare sunt peroxizi, EPA a conexiunilor (având gruparea funcțională - N = N -) și alți compuși cu legături slabe. Inițial radicali, de exemplu, format:
Apoi macroradicals formate, de exemplu, în polimerizarea clorurii de vinil:
R * + CH2 = CHCI ® RCH2 - * triclormetan
RCH2 - + CH2 = CHC CHC ® RCH2 - CHC - CH2 - CHC * etc.;
b) o creștere a lanțului are loc prin adăugarea la radicali monomeri pentru a produce radicali noi formate;
c) un transfer de lanț este transferul centrului activ în altă moleculă (monomer, polimer, molecule de solvent):
®R - (- CH2 -CHCl-) n + -SN2Sl -CH2CH = CHCI *
Ca rezultat, creșterea în lanț este terminată, iar molecula emițător, în acest caz, molecula de monomer inițiază o nouă reacție în lanț. Dacă transmițătorul este un polimer, poate să apară ramificarea lanț.
Etapa de terminare a lanțului este o interacțiune a radicalilor cu formarea unei molecule saturate valență:
de terminare a lanțului poate avea loc, de asemenea, în formarea radicalilor mai puțin activi, care nu sunt în măsură să inițieze reacția. Astfel de substanțe sunt numite inhibitori.
Astfel, reglarea lungimii și în mod corespunzător greutatea moleculară a macromoleculelor poate fi realizată utilizând inițiatori, inhibitori și alte substanțe. Cu toate acestea, transferul și terminarea lanțului pot să apară în diferite etape ale lanțului, astfel încât macromoleculele au o greutate moleculară diferită, adică, polidispersa. Polidispersibilitate este o caracteristică a polimerilor.
polimerizare radicală este un procedeu industrial pentru sinteza multor polimeri importanți, cum ar fi clorura de polivinil [CH SNSl-] n, polivinilacetatul [-CH2-CH (OSOSNz) -] n, polistiren [-CH2-CH (C6H5) -] n, poliacrilat [ -CH2-C (CH3) (COOR) -] n, polietilenă [-CH2-CH2-] n, polidiene [-CH2-C (R) = CH-CH2] n și diferiți copolimeri.
Ionic de polimerizare, de asemenea, are loc prin formarea de centre active, de creștere și de terminare a lanțului. Rolul centrelor active, în acest caz, joacă anioni și cationi. Prin urmare, există polimerizarea anionică și cationică. Inițiatorii de polimerizare cationică sunt compuși electrofili incluzând acizii protonici, cum ar fi H2SO4 și HCI, acid aprotic anorganic (SnCI4, TiCI4, A1Cl3 și colab.), Organometallic A1 (C2H5) 3 compuși și altele asemenea. Ca inițiatori de polimerizare anionică utilizate elekronodonornye substanță și un compus, incluzând metale alcaline și alcaline, alcoolați ai metalelor alcaline și altele. de multe ori, simultan cu ajutorul mai multor inițiatori de polimerizare.
Creșterea lanțului, puteți scrie ecuația reacției:
când polimerizarea cationică și
polimerizarea anionică a
Să considerăm, de exemplu, polimerizarea cationică a izo-butilenă cu inițiatori AlCl3 și H2O. forma recentă un complex
A1Sl3 H2O + „+ H [AlONSlz] -
Notând complexul cu formula H + X inițiază procesul de polimerizare poate fi reprezentat ca
Rezultantă cation complex, împreună cu o macroion formulare counterion X- care prevede lanțuri de creștere
CH3 CH3 CH3 CH3
H3C - C + X + H2C = C ®N3S ¾ C - CH2 - X-C +, etc.
CH3 CH3 CH3 CH3
Cu unele inițiatori complexe pot obține polimeri având o structură regulată (polimeri stereoregulate). De exemplu, un astfel de inițiator complex poate fi un complex de tetraclorură de titan și un trialchilaluminiu AIR3.
Metoda de polimerizare ionică este utilizată în producerea de poli-izobutilenă [-CH2-C (CHs) 2] n, polyformaldehyde [-CH2O-] n, poliamide cum ar fi poli-e-caproamide (nylon) [-NH- (CH2) 5- CO-] n, cauciucuri sintetice, cum ar fi cauciucul butadien [-CH2-CH = CH-CH2] n.
Metoda de polimerizare asigură 3/4 din volumul total al polimerilor produși. Polimerizarea se efectuează în vrac, soluție, emulsie, suspensie sau în fază gazoasă.
Polimerizarea în masă (în bloc) - acest monomer (i) lichid de polimerizare în stare nediluată. Acest lucru a condus la polimer suficient de pură. Dificultatea principală a procesului asociat cu îndepărtarea căldurii. Când soluția de polimerizare se dizolvă într-un monomer solvent. Atunci când un astfel de proces de polimerizare a îndepărta mai ușor căldura și controlul compoziției și structura polimerului, cu toate acestea, problema îndepărtarea solventului apare.
polimerizare în emulsie (polimerizare în emulsie) un monomer polimerizabil este dispersat în apă. Pentru a stabiliza emulsia în surfactanții mediu administrat. Metoda Demnitate - ușurința de îndepărtare a căldurii, posibilitatea de a obține polimeri cu greutate moleculară ridicată și o viteză de reacție ridicată, lipsește - necesitatea spălării polimerului din emulgator. O metodă utilizată pe scară largă în industrie pentru a produce cauciuc, polistiren, clorură de polivinil, acetat de polivinil, polimetilacrilat și altele.
Într-o polimerizare în suspensie (de polimerizare în suspensie), monomerul este sub formă de picături, dispregirovannyh în apă sau alt lichid. Perlele randamentele reacției polimerice variind de la 10-6 10-3 m dezavantaj al metodei. - Necesitatea de a stabiliza suspendarea și spălarea stabilizatorilor de polimer.
Când polimerizarea monomerului gazos este în fază gazoasă și produsul polimeric - în stare lichidă sau solidă. Metoda este aplicabilă pentru polipropilenă și alți polimeri.
sinteza polimer Polikondensatsiya.Reaktsiya din compuși având două sau mai multe grupe funcționale, însoțite de formarea de produși cu greutate moleculară mică (H2O, NH3, HCl, CH2O, etc.), se numește policondensare. contribuție semnificativă la studiul proceselor de condensare au oameni de știință români V.Korshak, G. Petrov și alții de oameni de știință străini - U.Karozers, P.Flori, P.Morgan compuși bifuncționali etc. policondensare numite liniare, de exemplu .:
® NH2- (CH2) 5-CO-NH- (CH2) 5-CO-NH- (CH2) 5-COOH + H2O etc.
Produsul final este poli-e-caproamide [-CO-NH- (CH2) 5] n. policondensarea compușilor având trei sau mai multe grupe funcționale cunoscute sub denumirea tridimensională. Un exemplu este tridimensională reacția policondensarea uree și formaldehidă:
NH2-CO-NH2 + CH2O ® NH2-CO-NH-CH2OH
NH2-CO-NH-CH2OH + CH2O ® CH2OH-NH-CO-NH-CH2OH
® H2O + CH2OH-NH-CO-NH-CH2-O-CH2-NH-CO-NH-CH2OH
Prima etapă este sintetizat oligomerului structură liniară:
Într-o a doua etapă, prin încălzire într-un mediu acid are loc policondensarea în continuare a oligomerului cu eliberare CH2O și plasă apariție structura:
- N-CH2-N - CH2-N - CH2-N-CH2-CH2-N -
÷ ÷ ÷
÷ ÷ ÷
- N -CH2¾N CH2-N-CH2-CH2-N-N-CH2 -
Un astfel de polimer nu se poate transforma, în starea inițială, nu are proprietăți termoplastice și este numit polimer termorigid.
De asemenea, considerate o legătură chimică între monomeri în timpul policondensării apar prin alte legături chimice între monomerii grupe, dintre care unele sunt cuprinse în tabelul nr. 14.1.
Tabelul 14.1. Legăturile chimice dintre grupările funcționale ale unor monomeri care apar la policondensarea lor
Deoarece în timpul policondensării, împreună cu produsele de formă cu greutate moleculară mică moleculară mare, compoziția elementară a materiilor prime și a polimerilor nu se potrivesc. Aceasta diferă de polimerizarea policondensare. continuă policondensare printr-un mecanism în trepte, produsele intermediare sunt stabile, adică, Policondensare se poate opri în orice stadiu. Rezultate produse de reacție cu greutate moleculară mică de (. H2O, NH3, HCl, CH2O, etc.) poate fi reacționat cu intermediarii policondensare care cauzează clivaj lor (hidroliză, aminoliza, acidoliză și colab.), De exemplu:
Prin urmare, produsele cu greutate moleculară mică trebuie îndepărtată din mediul de reacție.
Compușii monofuncționali prezenți în mediul de reacție, să reacționeze cu produse intermediare pentru a forma compuși nereactivi. Acest lucru duce la întreruperea lanțului, deci monomeri pornind trebuie să fie libere de specii monofuncționale. Compușii monofuncționali pot fi formați în timpul reacției din cauza căldurii sau de degradare oxidativă intermediari. Aceasta conduce la o oprire reacția de policondensare și pentru a reduce greutatea moleculară a polimerului.
Policondensare se realizează fie în topitură sau în soluție sau la interfață.
Policondensarea în plumb topitură fără solvent, prin încălzirea monomerilor la o temperatura la 10-20 ° C peste punctul de topire (înmuiere), polimeri (de obicei, 200-400 ° C). Procesul începe într-o atmosferă de gaz inert și se termină în vid.
În policondensarea în soluție folosind un solvent care poate servi ca un produs absorbant moleculară mică.
policondensare interfacială are loc la interfața gaz - o soluție sau două lichide nemiscibile și produce polimeri cu greutate moleculară mare.
Metoda policondensare oferă aproximativ un sfert din polimerilor produși, de exemplu, poli-e-caproamide (nylon), poli-geksametilenadipinamid (nylon) [-NH (CH2) 6NHCO (CH2) 4CO-] n, poliesteri (polietilen tereftalat [- (- OS) C6H4 (CO) OSN2SN2-] n), poliuretani [-OROCONHR'NHCO-] n, polisiloxani [-SiR2-O-] n, poliacetali [- OROCHR „-] n, rășini fenol-formaldehidice